人工知能(AI)、ビッグデータ法務 ヘルスケア スタートアップ 未分類
【AI医療機器開発連載・第1回】AI医療機器の開発からサービス提供までの流れと法規制・契約

本記事は「【連載】法規制、契約、知的財産の観点から見るAI医療機器開発」の第1回目の記事です。
【連載】法規制、契約、知的財産の観点から見るAI医療機器開発
第1 【第1回】AI医療機器の開発からサービス提供までの流れと法規制・契約
第2 医療データ収集段階の規制と契約
1 【第2回】AI医療機器開発のための医療データ収集と個人情報保護法
2 【第3回】AI医療機器開発に関する臨床研究・医学系研究関連規制
第3 AI医療機器開発・ハードウェア製造段階の規制と契約
第4 治験・薬事承認・保険収載段階の規制と契約
第5 サービス提供段階の規制と契約
連載第1回目の本記事では、AI医療機器の開発からサービス提供までの流れと法規制・契約の全体像について簡単に説明をします。
AI医療機器の開発からサービス提供までの流れと法規制・契約の全体像を示したのが下図です。
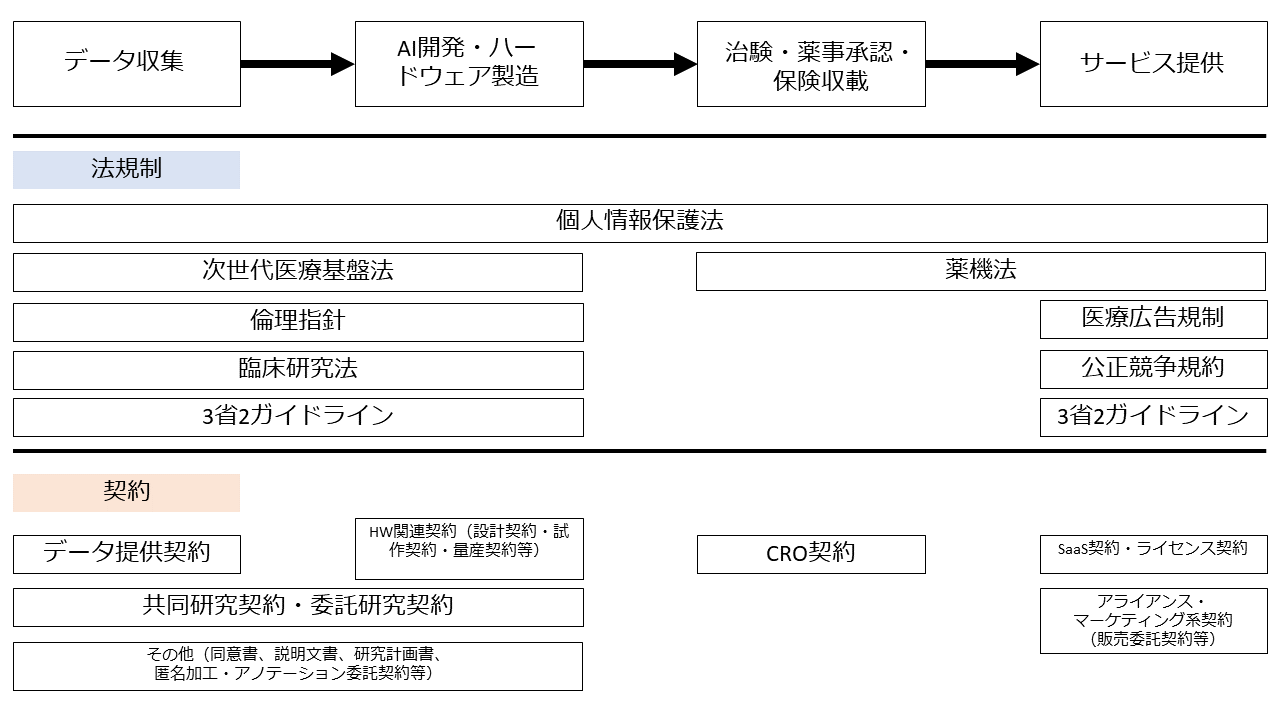
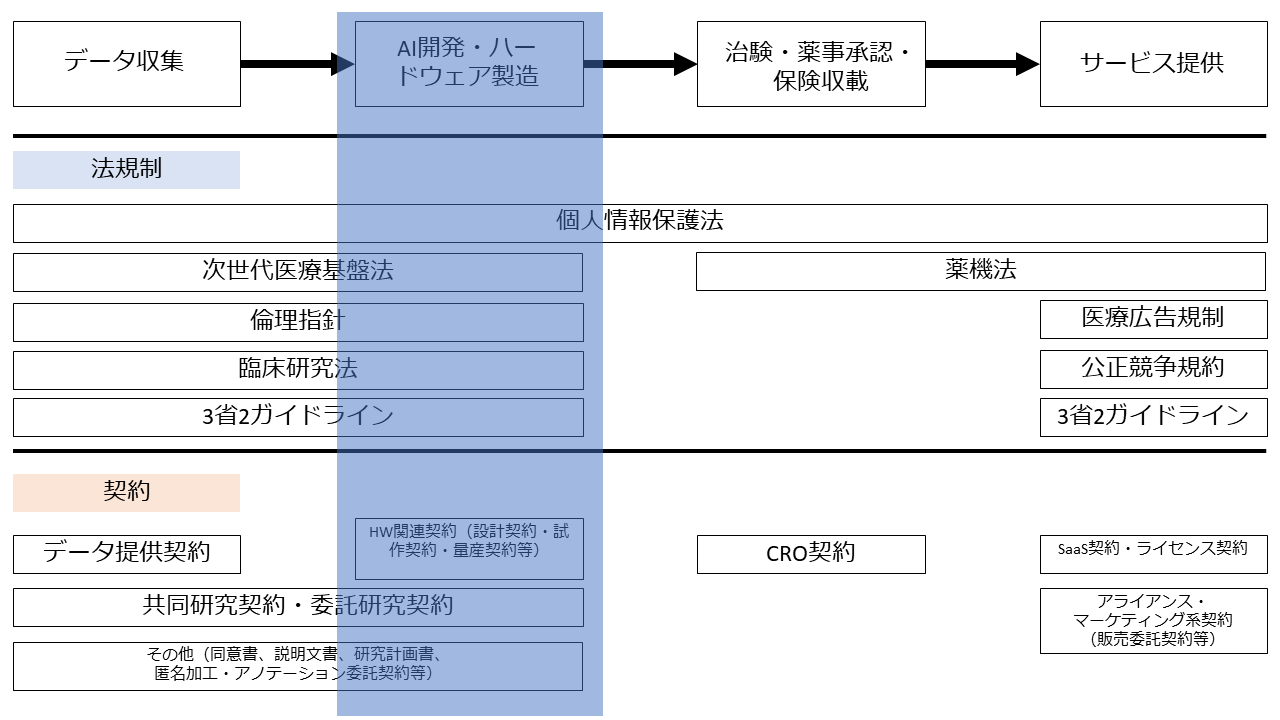
この図では、フェーズを時系列に従って「データ収集」「AI開発・ハードウェア製造」「治験・薬事承認・保険収載」「サービス提供」の4つに分け、各フェーズで問題となる法規制と契約についてプロットしています。
もっとも、これら4のフェーズは密接に関連していることに注意が必要です。
たとえば、AI 医療機器については、変更計画確認手続制度(IDATEN:Improvement Design within Approval for Timely Evaluation Notice)の利活用が期待されていますが、IDATEN 制度の利活用を見据えるのであれば、研究開発当初より、市販前から市販後までのトータルの研究開発計画や医療機関との医療データの共同利用計画の策定が必要とされています1 https://www.meti.go.jp/shingikai/sankoshin/shomu_ryutsu/bio/kojin_iden/life_science_tf/pdf/006_s02_00.pdfのP15 。これは一例ですが、先行するフェーズ(データ収集等)の段階において後行するフェーズ(薬事承認手続やサービス提供)のことも考えておく必要があり、各フェーズを分断して検討するのでは不十分であるということになります。
以下、各フェーズの概要について説明をします。
1 データ収集
まず、AI医療機器開発に必要なデータ収集フェーズについてです。
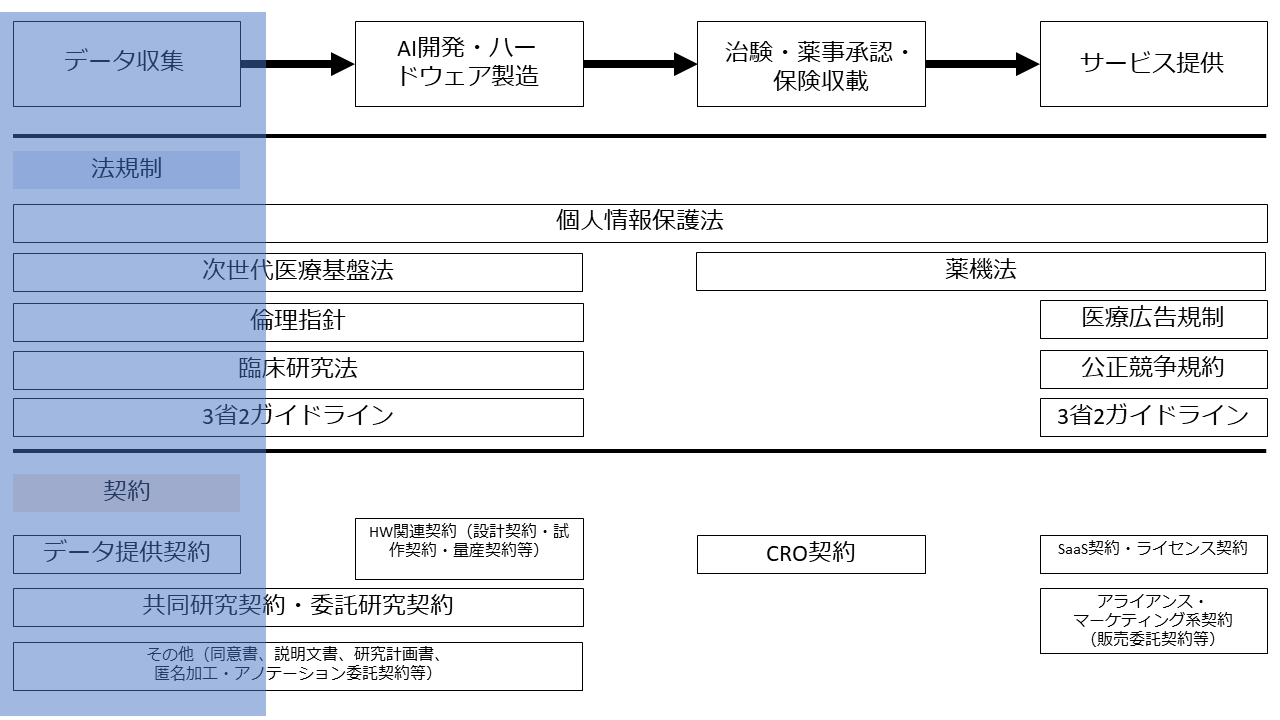
(1) 法規制
AI医療機器開発においては、高品質な医療データを大量に収集することが極めて重要ですが、ここでの「医療データ収集」の流れは、通常は「患者さん本人→医療機関」と「医療機関→AIベンダ」の2つを意味しています。つまりAI医療機器開発においては、医療機関は患者さんから取得した医療データをAI医療機器開発のためにAIベンダに提供していますし、AIベンダは医療機関から患者さんのデータを収集(取得)していることになります。
そして、医療データは「個人情報」に該当しますので、その収集や提供に関しては大きく分けて個人情報保護法上の規制と倫理指針・臨床研究法上の規制がかかります。
個人情報保護法上の規制については、個人情報の収集や提供をどのようなスキームで適法化するかという問題です。実務的には様々なスキームが存在しそのメリット・デメリットを理解することが重要です。また、同様に個人情報の適正な収集という点においては次世代医療基盤法のスキームを利用することも考えられます。
次に、倫理指針・臨床研究法はざっくり言うと、ヒトを対象とした医学系研究を行う場合に適用される規制です。その規制はデータ収集から当該データを用いたAI開発まで広く及びます。
さらに開発したAI医療機器をクラウドサービスとして提供する場合には、いわゆる3省2ガイドラインを遵守する必要がありますので、その点についてもデータ収集段階から注意が必要です。
(2) 契約
医療データ収集のフェーズにおいては、医療機関から医療データの提供を受けるに際してのデータ提供契約が締結されることがあります
また契約書以外の書類としては、医療機関が患者さんに対するICを行ったり同意取得をする際の同意書・説明文書や、倫理審査委員会に提出するための研究計画書などが必要となりますので、それらについても必要な範囲で解説いたします。
2 AI開発・ハードウェア製造
次にAI開発・ハードウェア製造フェーズです。
(1) 法規制
AI開発では収集した大量の医療データを用いてAIモデルを開発することになりますので、個人情報を利用したソフトウェア開発という側面と、ヒトを対象とした医学系研究という側面の2つを有することになります。そのため、「データ収集」のフェーズと同様、個人情報保護法、次世代医療基盤法、倫理指針、臨床研究法及び3省2ガイドラインが問題となります。
(2) 契約
次に、AI医療機器開発においては医療機関と医療機器メーカー、AIベンダが協力して開発を行うことも多いのですが、その場合両者の間でデータ提供契約、共同研究契約、委託研究契約、匿名加工委託契約等の各種契約を締結することになります。
それらの契約においては各自の役割分担や費用負担などが定められることになりますが、契約条項として重要なのは、研究過程で得られたデータの利用権限及び成果物であるAIモデル等の知的財産権の帰属や利用条件です。データやAIモデルの知財についての合意内容は、開発後の展開方法や収益性に大きく影響するためです。
さらにAI医療機器開発においては、ソフトウェア(AI)の開発と並行してハードウェアの開発・製造も行われることがありますが、両者は全く異なるものです。
ハードウェア製造においては、要件定義・原理試作・量産設計・量産試作を経て初めて量産プロセスにたどり着くことができることや、スタートアップの場合は設計・製造業者などものづくり関連業者との間での協業が不可欠という特徴があるためです。
そのため、ハードウェア製造については独立して解説の対象とする予定です。
3 薬事承認・保険収載
さらに、薬事承認・保険収載フェーズです。
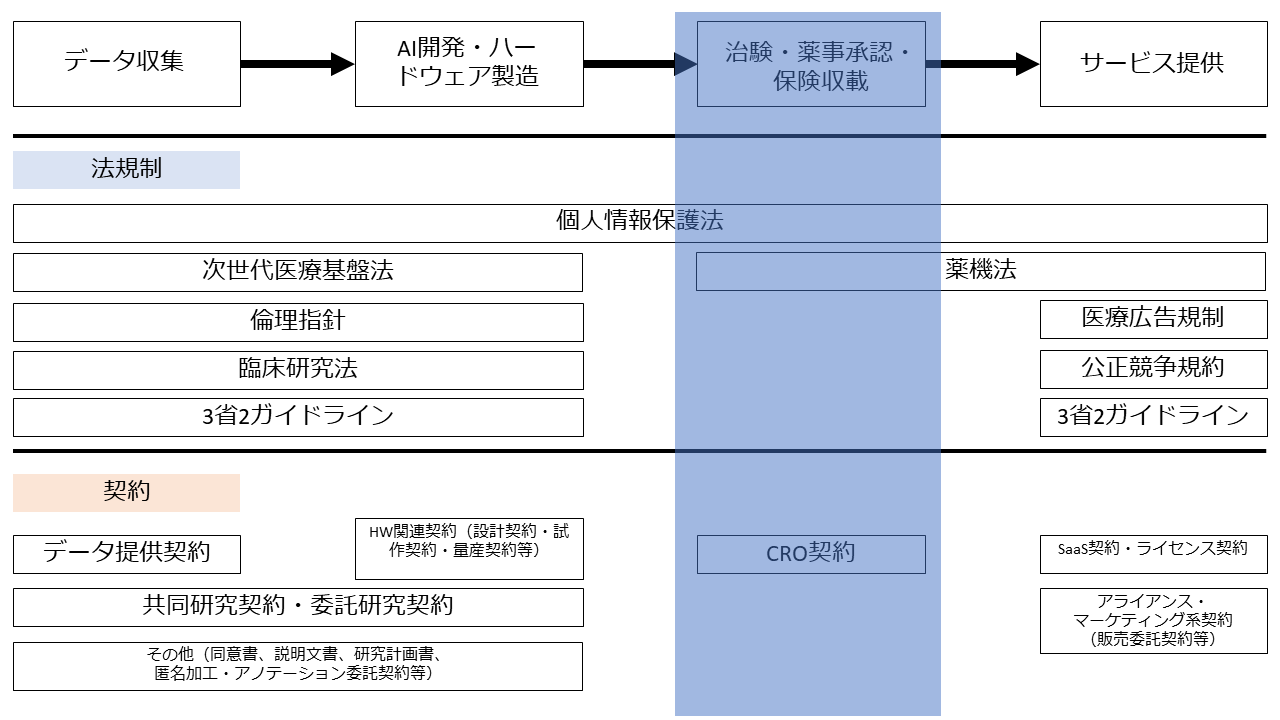
ソフトウェアだけで構成されているAI医療機器はプログラム医療機器の一種ですが、AI医療機器の特徴として、①最終結果を導き出すアルゴリズムがブラックボックス化している、② 市販後学習等による性能変化が可能である点が指摘されています。
そのような特徴を踏まえて、AI医療機器の承認審査上は様々な点が通達(「次世代医療機器評価指標の公表について」(令和元年5月23日・薬生機審発0523第2号))等で明らかにされているところです。
4 サービス提供
最後にサービス提供フェーズです。
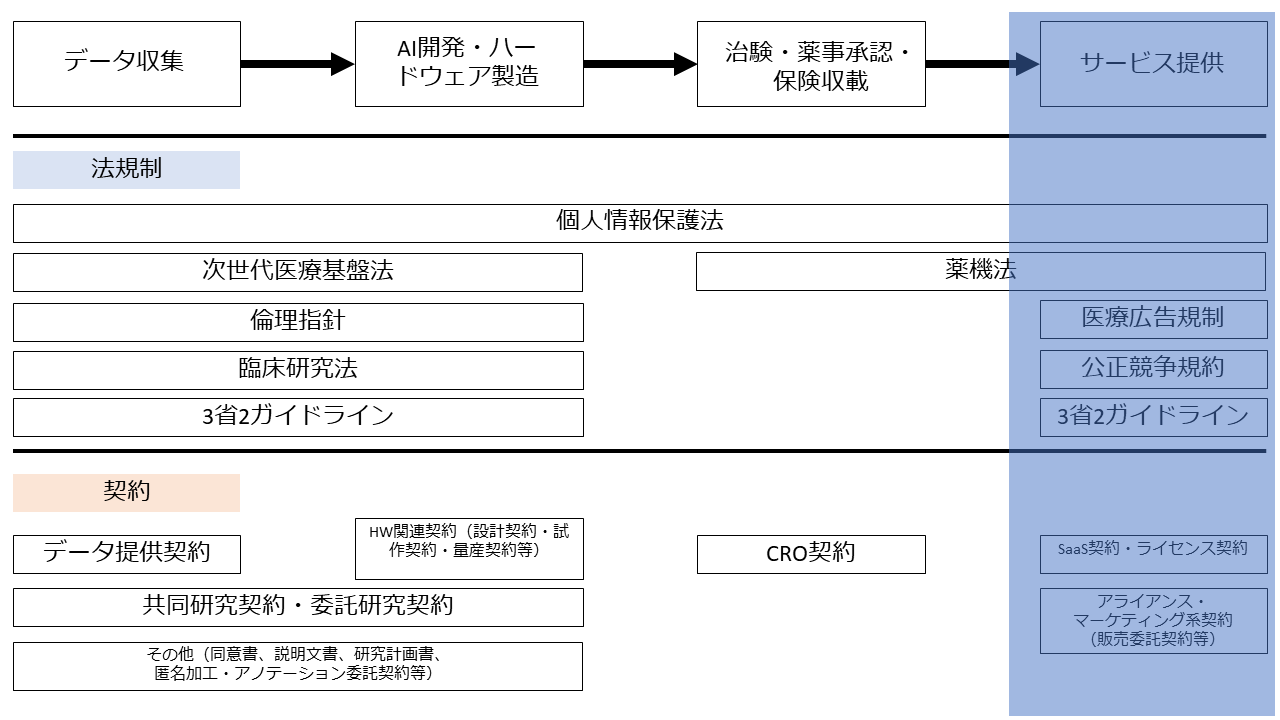
開発が完了したAI医療機器は市販していくことになりますが、そこでは医療機器の提供やマーケティングに関する法的規制(3省2ガイドライン、医療広告規制、公正競争規約)をクリアする必要があります。
この段階における契約関係としては、まず医療機関との間のSaaS契約やライセンス契約等、サービス提供そのものに関する契約が必要です。通常のSaaS契約の内容にプラスして、処理対象としている医療データの扱い(追加学習等に利用することが可能か等)についても定める必要があります。
さらに医療機器の販売に際して締結されるアライアンス・マーケティング系契約(販売代理契約等)についても解説します。
■ 「【連載】法規制、契約、知的財産の観点から見るAI医療機器開発」の目次はこちら